文:王蕾 沈炯
來源:峰瑞資本(ID:freesvc)
1835 年,達爾文登上加拉帕戈斯群島,開始自己的發現之旅。他采集了大量珍貴的標本,其中就包括群島上特有的一群雀。它們有相近的喙的結構、短尾、體型和羽毛形狀。
1839年,達爾文在《小獵犬號航海記》中寫道:“看到如此極小的一群、非常近緣的鳥的結構之漸變和多樣化,人們或可想象這個群島最初沒有什么鳥,一個物種被修修改改以滿足不同的目的。”
正如那些為了適應環境而不斷演化的雀,人類也在與時間的賽跑中不停尋求適應與進化之道。關于衰老的科學探索,就是其中之一。
衰老,作為人類生命進化過程中的伴隨產物,已經成為老齡化時代我們必須正視的現實。到 2050 年,全球超過 65 歲的人口將占總人數的六分之一。
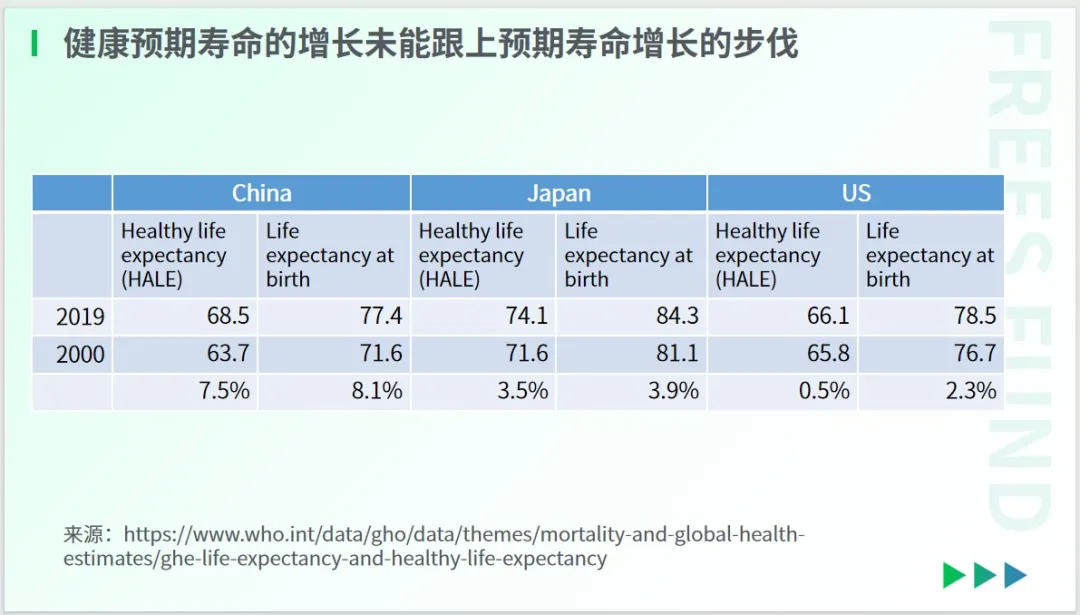
與此同時,人類的“健康壽命”并沒有跟上壽命延長的步伐——多數人在六七十歲時,便陷入帶病衰老的困境。
因此,抗衰的目標,并非對抗死亡,而是“延長健康壽命”,減少患病、失能的發生。
不過,如何延長健康壽命是個古老、復雜的議題。古時帝王追求仙藥,以求長生,今時豪客嘗試換血,以續青春。
從早期投資的視角出發,我們始終關注與衰老和老齡化相關的疾病,并持續對相應的解決方案進行投資。
近年來,得益于科學研究的深入和生物技術的突破,很多關于衰老的謎題得以破解。我們也把注意力從老齡化相關的疾病,轉移到衰老過程本身,以及那些試圖抵抗衰老的創新方法。
醫美,在一定程度上可以幫助皮膚抗衰。從傳統的“管住嘴邁開腿”到注射司美格魯肽,是生物科技在體重控制領域發揮神奇作用,而體重控制有助于抗衰。此外,細胞與基因療法雖面臨爭議,但也已屹立于抗衰科研的前沿。
在本文中,我們將回到生物世界的第一性原理,探究衰老及與之相關的概念——出生率、壽命。此外,我們系統梳理了與衰老相關的科學和醫學進展,以及現實挑戰,以期能科學地審視衰老。我們探討的話題涵蓋:
-
生物世界的第一性原理是什么?
-
如何定義衰老?衰老是一種病嗎?
-
衰老的標志有哪些?
-
關于抗衰,目前科學和醫學分別走到了哪一步?
-
如何科學地抗衰?
-
當我們討論抗衰的時候,有哪些新語境與新議題?
-
抗衰的未來會是什么樣?
我們整理了與抗衰有關的重點書目和論文,已放在文末,供你參考。

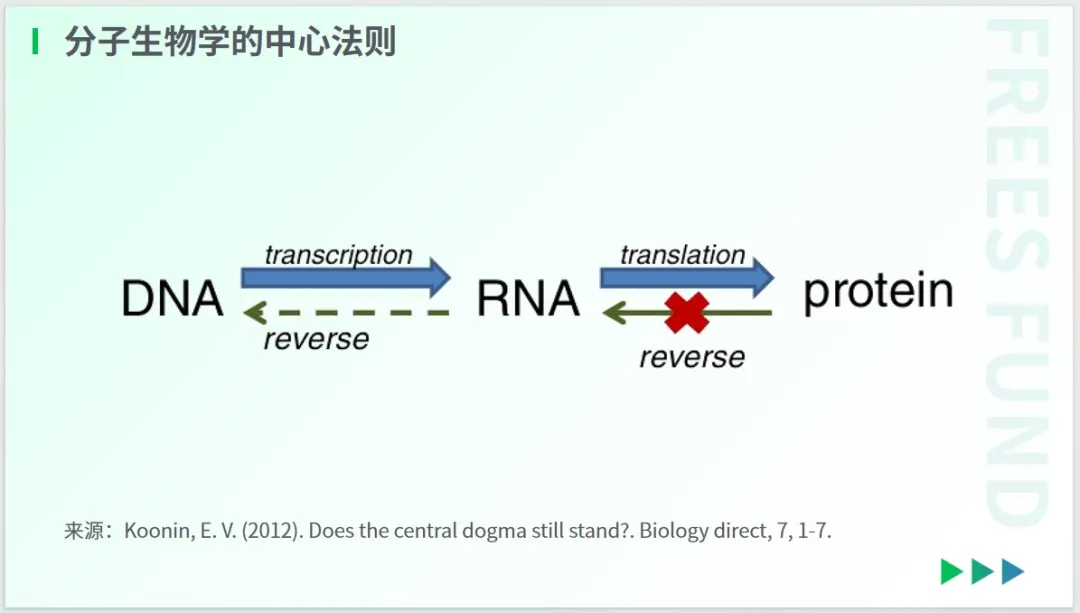
1958 年,佛朗西斯·克里克提出了分子生物學的中心法則,即遺傳信息在不同的大分子之間的轉移都是單向、不可逆的,只能從 DNA 到 RNA(轉錄),從 RNA 到蛋白質(翻譯)。
這兩種形式的信息轉移,在所有生物的細胞中都得到了證實。
然而,60 多年后的今天,盡管生物技術高度發達,我們對人體的理解還遠不足夠,很多事情仍然像是“黑箱”。比如,在創新藥的研發過程中,若未經大規模臨床試驗,幾乎無人能預判其安全性與有效性。
與物理世界嚴密的邏輯規律不同,在生物世界里,我們難以用演繹推理的方法對生物體進行準確預測。
具體而言,即便對于同一物種,即使我們研究發現了細胞的某一條信號通路,也常常無法借此預測或解釋其他信號通路的運行邏輯。
那么,生物世界的第一性原理究竟是什么?
這便要回溯到一個經典理論——達爾文的進化論。物競天擇,適者生存。
正如開頭所提及的,雀的形態經過漫長歲月的“改良”,才適應了島上的自然環境。與此同時,哪些幫助雀熬過極端環境的特征會被遺傳給下一代。就這樣,在“適者生存”的進化法則之下,生命在“有改變的繼承”中代代延續。
在生命進化的歷程中,死亡是必然產物,而衰老則是生命進化過程的伴隨產物,且它與壽命的進程緊密相關。

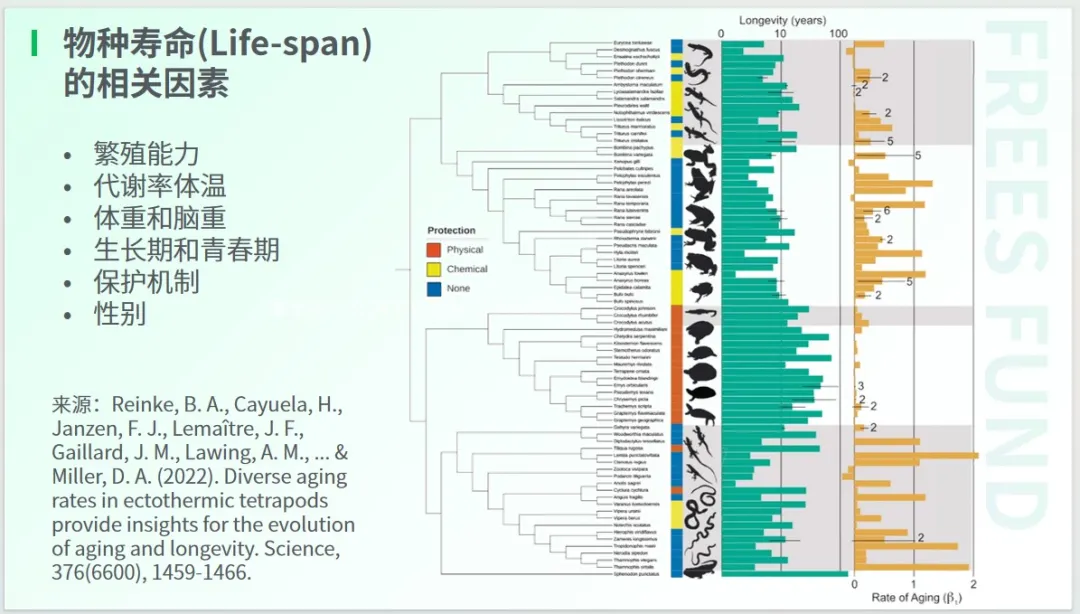
物種的壽命與繁殖能力、代謝率、體溫、體重、性別等諸多因素密切相關。
這里有一些有趣的事實:
-
保護機制方面:爬蟲動物的壽命長短不一,長則上百年,短則僅數月至一年。研究發現,最長壽的爬蟲動物主要有兩類,一類是有甲殼的,如烏龜;另一類是有毒液的,以蛇為例,有毒的蛇往往比無毒的蛇壽命更長。
-
性別因素方面:與人類不同,雄性鳥類通常比雌性壽命更長。這是因為鳥類與哺乳動物不同,其雄性擁有兩個相同的性染色體。
-
繁殖能力因素方面:經過自然選擇或人工篩選后,壽命長的果蠅聚集在一起,繁殖力會下降,而壽命短的果蠅聚集后,繁殖率會提高。這意味著延長壽命的代價是生殖能力的下降。
不過,科學家總結出的這些因素,并不能絕對地代表因果關系,而只是在一個復雜的系統中找到了不同因素的相關性。
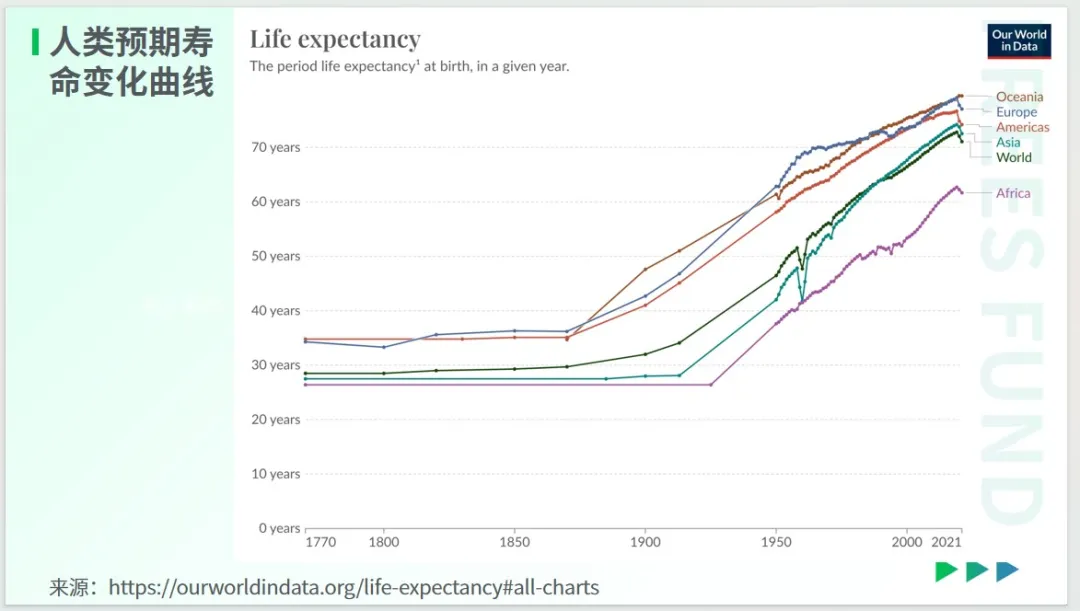
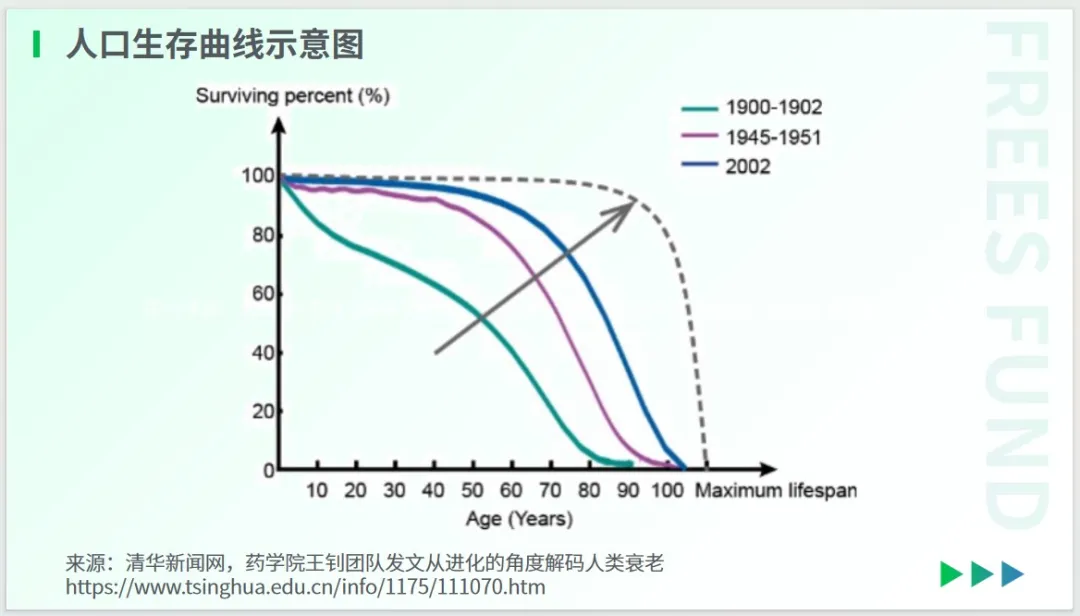
從上面的圖表中我們可以看出,人類壽命的大幅提升,始于 20 世紀上半葉,這與公共衛生的進步密切相關。其中,新生兒死亡率的下降,對過去一個世紀人類預期壽命的增長貢獻卓著。
具體到不同地區,我們會發現,歐洲人均壽命在 18 世紀時就已超越其他地區,這大致得益于工業革命帶來的一些變革。
在這張圖表中,加拿大東部出現了偏離值,在歐洲殖民者抵達北美大陸之前,生活在該地的古人就有長壽的記錄。即便沒有任何科技的加持,他們中的許多人能活到 80 歲,甚至不少人能活到 100 歲。
關于人類壽命的極限,當前主要有兩種觀點。
其一為性成熟理論,依據統計學推論,人類壽命的極限是性成熟年齡的 8 - 10 倍。由于人的性成熟大致發生在 15 歲左右,因此人類的極限壽命為 120 歲。
另一種說法是海夫利克極限,即細胞分裂的極限為 50 次。體細胞分裂的平均周期為 2.4 年,分裂 50 次,結論同樣是 120 歲。

對動物界而言,繁育和傳承是進化的主要目標,自然選擇通常只作用于那些可提高繁殖成功率的基因。許多動物包括靈長類動物在完成了繁殖之后,或者說失去繁殖能力后,很快就會走向生命的終結。
人類卻是個例外。
人類在繁殖期結束后,仍會延續相當長的生命,這段生殖期后壽命(Post-reproductive lifespan,PRLS),即所謂的衰老期。
這意味著,人類的衰老并非自然選擇的結果,而是源于人類社會的選擇。至于人類為何會如此選擇,目前尚無確切解釋。
有一種說法認為,衰老期對人類是有益的。這主要體現在兩個方面:
其一,人類是社群動物,親情的照顧有助于整個社群的穩定。在動物界也有類似例證,例如,蜂群中蜂王的壽命特別長,是因為整個蜂群都在照料它,而親情照顧有利于蜂群的穩定,蜂王的長壽就是這個機制的副產品。
另一方面,在進化上,人和其他動物相比,優勢并不在于體力,而是腦力和智力。因為神經元是不會死亡的,理論上,在沒有疾病的情況下,一個人的智力認知會隨著壽命增長而增長。從這個意義上說,盡可能延長生命,對人類是一種正向的選擇。
“衰老”這一專屬于人類的社會性概念,也是一個極為年輕的概念。
因為在 200 多年前的 1800 年,人類的平均壽命尚不足 40 歲。饑餓、疾病、殺戮以及各種災難,使得人類可能尚未進入衰老期便已遭遇死亡。
近幾十年來,得益于社會經濟、公共衛生、醫藥保健等領域的發展,以及世界環境的相對和平,人類的預期壽命有了顯著提升,我們才有機會目睹越來越多的“衰老”現象。
當老齡化已然成為不可避免的趨勢,且“健康壽命”并未跟上壽命延長的步伐,抗衰成為一個重要的議題。盡管在相當長的時間里,關于衰老本身是否是一種病的爭論還在繼續。
2018 年,世界衛生組織(WHO)曾將衰老納入疾病范疇,但在其最新的國際疾病分類(ICD - 11)中,衰老被描述為“內在能力的衰退”,卻并未明確將其定義為疾病。
WHO 的這種描述,承認了衰老的生物過程,為開發針對衰老的治療方法提供了基礎。當下的共識是,抗衰的目標并非對抗死亡,而是“延長健康壽命”,減少患病和失能的發生。

在歷史長河中,人類一直致力于理解和對抗衰老。
古人發明草藥療法和針灸技術,以期促進健康與長壽。此類故事我們都耳熟能詳。
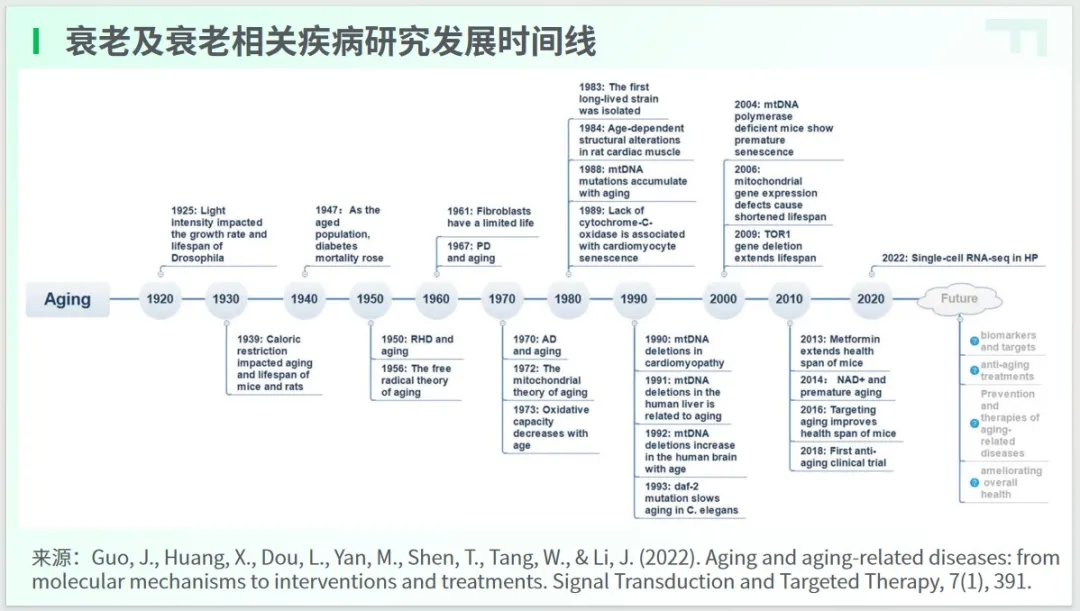
自 20 世紀 20年代起,研究者們通過實驗證實,動物的壽命是可以調控和影響的。例如,實驗結果表明,在不同光照條件下,果蠅的壽命存在顯著差異;限制卡路里的攝入,能夠延長小鼠和大鼠的壽命。
1950 年代以來,隨著遺傳學的發展以及生物技術的不斷突破,人類對衰老和抗衰的認知逐漸深化。
在時間維度上,人們相信通過增加健康壽命的時長,“衰老期”可以被壓縮;在空間層面上,研究者期望通過減少疾病和失能,改變或延緩“衰老”特征,即所謂的“抗衰”。
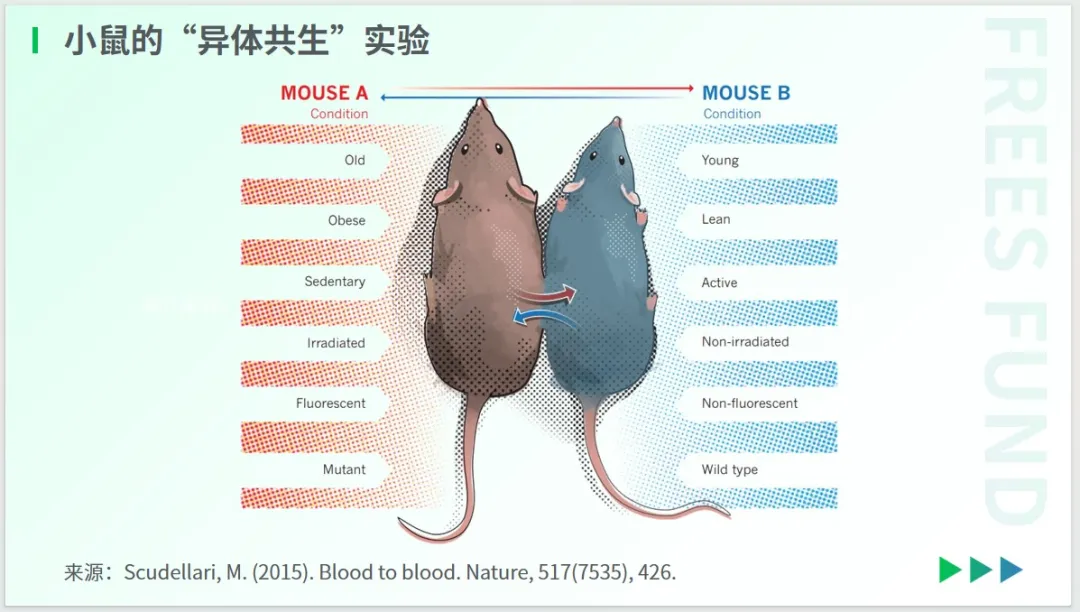
在抗衰領域,“異體共生”實驗備受關注——通過人工設計和手術,使兩個活體動物(一者年輕,一者年邁)共享血液、器官和環境。
2005年,美國學者Conboy夫婦在《Nature》上發表的研究指出,年輕小鼠的血液能夠改善年老小鼠的肌肉和肝臟的再生能力,在一定程度上逆轉老年小鼠的衰老跡象。
這項試驗激發了后續的大量研究,也相繼得到了多次驗證。2015年,知名科學記者Megan Scudellari在《Nature》發文說:通過將動物拼接在一起,科學家們已經證明,年輕的血液可以使衰老的組織恢復活力,接下來要做的事情是,測試它是否適用于人類。
總體而言,“異體共生”對人體的生物學年齡和長期健康的總體影響尚不清楚。但為了“返老還童”,總有人愿意嘗試。
硅谷富豪布萊恩·約翰遜(Bryan Johnson)的“嗜血”抗衰故事廣為人知。曾有一段時間,在加州蒙特里,一家名為 Ambrosia(中文意為“不朽”)的公司診所內,人們只需支付 8000 美元,便可采用“年輕血液”抗衰老療法。2017 年播出的美劇《硅谷》第四季中,就出現了“換血抗衰”的劇情。
2019 年,該療法被?美國食品和藥物管理局(FDA) 一紙禁令叫停。即便如此,類似的研究并未停止。
2022 年 8 月,Conboy夫婦在《GeoScience》發表論文稱,在人衰老的過程中,體內會積累許多代謝廢物,或許我們無需進行“異體共生”,只需將自身體內的血液稀釋一半,便可達到“變年輕”的效果。
不過,此次小樣本人體試驗的結果,能否在未來更大規模的研究中重現,仍有待觀察。
總體而言,衰老頗為復雜。人類對“老而不衰”的無盡追求,將繼續推動與衰老相關的科學和醫學不斷向前發展。

那么,衰老究竟是如何發生的?衰老是基因決定的嗎?衰老又是從何時開始的?接下來,我們會深入探究衰老的底層機制與理論,以助大家更好地理解衰老的發生過程。
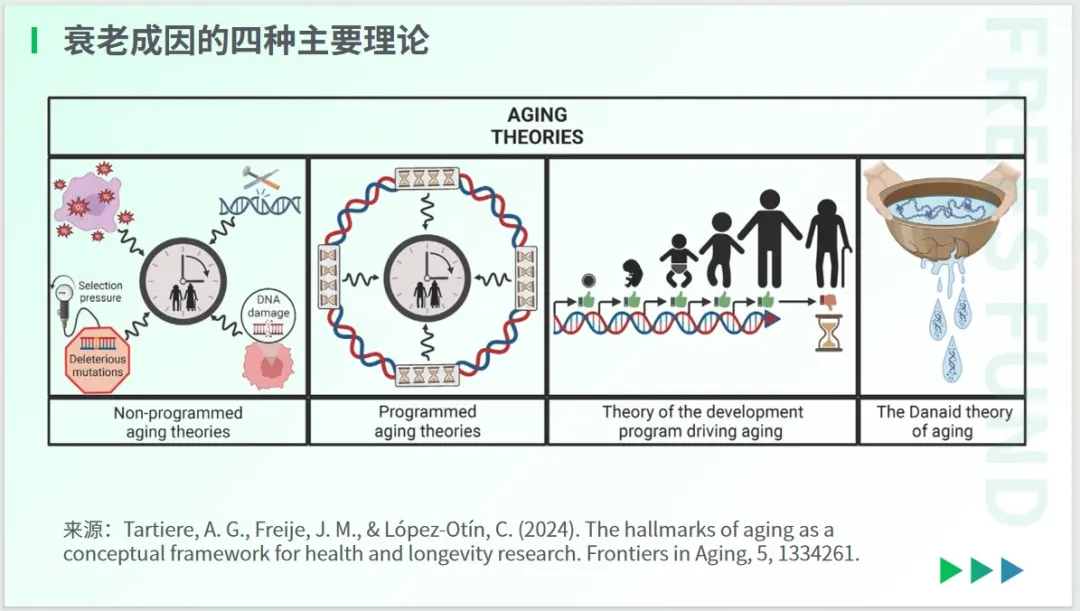
關于衰老的成因,當前學界存在四種理論:非程序性衰老理論、程序性衰老理論、發展程序驅動衰老理論以及達奈德衰老理論。
非程序性衰老理論主張,生命中累積的損傷推動了衰老過程的發生。程序性衰老理論則認為,特定的遺傳程序是推動“衰老時鐘”的關鍵因素。
介于這兩種觀點之間,發育程序驅動衰老理論提出,發育程序的缺陷是導致衰老的主要驅動力。
與之類似,達奈德衰老理論認為,衰老是生物學的固有結果。該理論借用希臘神話中的達奈德(Danaids)來隱喻衰老。在希臘神話中,達奈德因謀殺丈夫而被判處永遠用穿孔容器裝水。
從這個角度來說,該理論認為生物體就如同穿了孔的容器,其生物學固有的缺陷(孔)使得它無法永遠容納生命(水)。
類比到人類,當最底層的細胞開始出現一個個“洞”時,這些變化會體現在人體的各個器官上,包括皮膚、神經、骨骼等,從而呈現出不同程度的衰老。

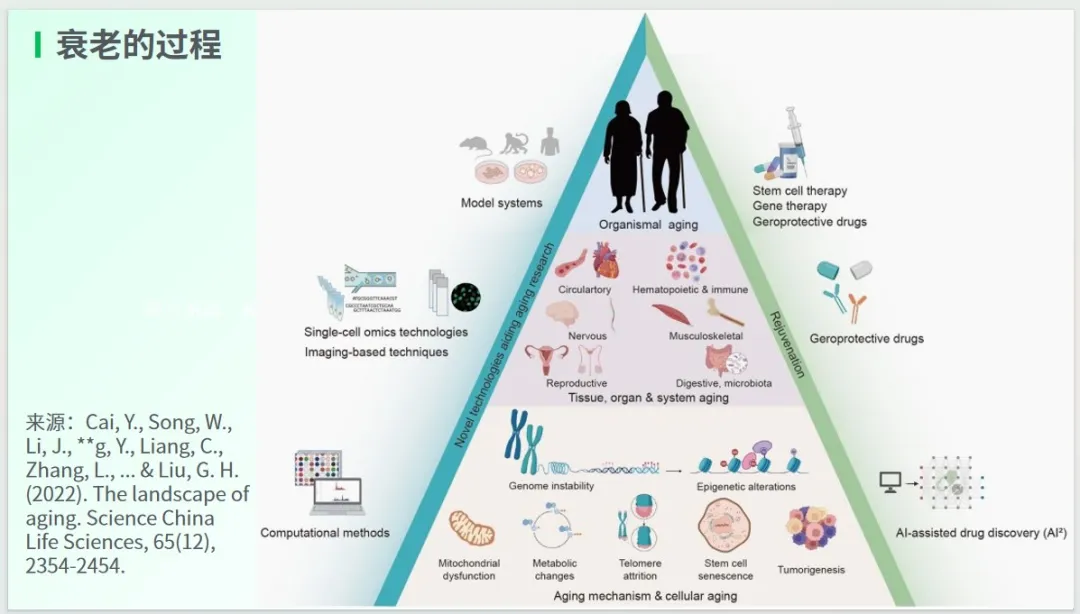
透過下圖中的“金字塔”,我們能夠清晰地一覽衰老過程發生的全景。
在金字塔的最底端,是微觀層面的細胞衰老;中間部分,則是中觀層面的組織、器官與系統的衰老;而最上面,則是宏觀層面的機體衰老。
這與上文所提及的達奈德衰老理論高度契合。衰老就如同在分子和細胞這樣的底層出現了一個個“洞”(缺陷),這些缺陷在人體的多個器官上有不同程度的體現,進而引發了不同程度的器官衰老,最終導致整個人的“衰老”。
金字塔的左邊展示的是衰老的研究方法,涵蓋了生物模型系統、單細胞組學技術、基于成像的技術、生物計算方法等。與之相對應的金字塔右邊,則是衰老的治療方法,包括干細胞治療、基因治療、抗衰老藥物以及人工智能輔助藥物發現等。

回歸到最微觀的分子和細胞層面,2023 年 1 月,西班牙奧維耶多大學的 Carlos López-Otín 以及法國古斯塔夫魯西研究所的 Guido Kroemer 等人在《Cell》上發表了一篇題為“Hallmarks of aging: An expanding universe”的綜述文章,對衰老的十二大特征進行了定義并予以詳細闡述。
作者指出,衰老標志必須滿足以下三個標準:(1)會隨年齡的增長而發生變化;(2)在實驗中增強該特征,有可能加速衰老;以及最為重要的一點(3)通過對該特征進行治療和干預,有可能減緩、停止甚至逆轉衰老。
這 12 個衰老特征包括:基因組穩定性喪失、端粒損耗、表觀遺傳改變、蛋白穩態喪失、營養感應失調、線粒體功能障礙、細胞衰老、干細胞耗竭、細胞間通訊改變、大自噬功能失效、慢性炎癥以及生態失調。
值得一提的是,前 9 個特征是作者在 2013 年就已提出的,而后 3 個則是此次新添加的。
作者還將這些特征分為了三類:原發性、拮抗性、綜合性。
衰老的基礎標志,即原發性標志,是啟動衰老過程的關鍵。因為它們所產生的損傷會隨著年齡的增長而不斷累積。
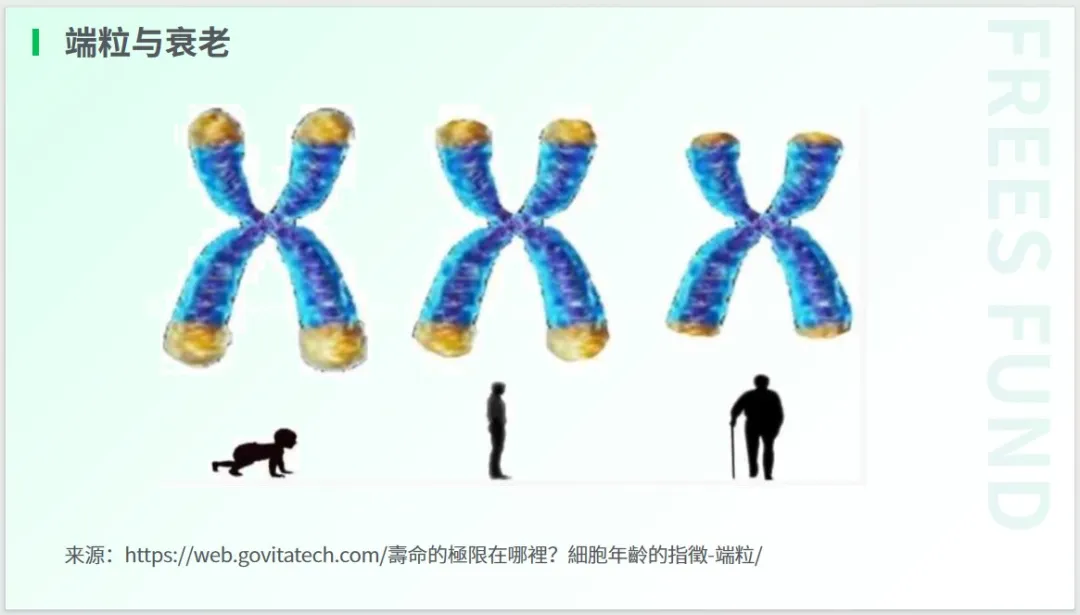
以端粒損耗這一原發性標志為例。研究表明,端粒長度與衰老、人種、分布組織、遺傳和變異等諸多因素存在關聯。
如前所述,按照海夫利克極限計算,人體細胞大約能夠分裂 50 次。隨著細胞分裂次數的增加,人類端粒每次會縮短約 40 - 200 個堿基對(bp),因此,在衰老死亡之前,端粒長度通常會剩余一半左右,約為 5 - 6 kb。
2009 年,諾貝爾生理學與醫學獎就頒發給了三位研究端粒的科學家,他們因在端粒和端粒酶如何保護染色體方面的發現而獲此殊榮。在抗衰領域,我們也可以看到許多研究是從增加端粒長度這一角度入手的。
此外,許多與年齡相關的神經退行性疾病,諸如漸凍癥和阿爾茨海默癥,都可能與蛋白質穩態受損有關。蛋白質穩態的劇烈擾動,會加速身體的衰老進程。
拮抗性指的是最初對人體有益的機制或通路,隨著時間的推移,逐漸變得對人體有害。前面所提及的原發性因素帶來的損害逐步累積,也會加劇這一過程。簡單來說,年輕時的“蜜糖”,到年老時卻成了“毒藥”。
以營養感應失調為例。當細胞判斷營養素存在與否的機制失效時,營養素感應失調便會發生,從而帶來有害影響。
要知道,在人處于發育期時,或者說在極端惡劣的環境中,我們的身體會創造出一種機制來制造營養,以保護細胞免受營養素匱乏的影響,從而使我們得以生存。
因此,有學者提議從能量控制的角度來抗衰,相當于人為營造一個環境,讓身體感受到一種類似于人在發育期對營養有渴求的狀態,以延緩營養感應失調,保持旺盛的生命力。
類似地,還有研究者提出以適度寒冷來抗衰,因為這樣可以激發人年輕時的保護通路,以期達到抗衰的效果。
當原發性和對抗性特征造成的累積損傷無法抑制或修復時,整合標志就會出現,導致干細胞衰竭、細胞間通訊改變。它們共同決定了衰老的速度。

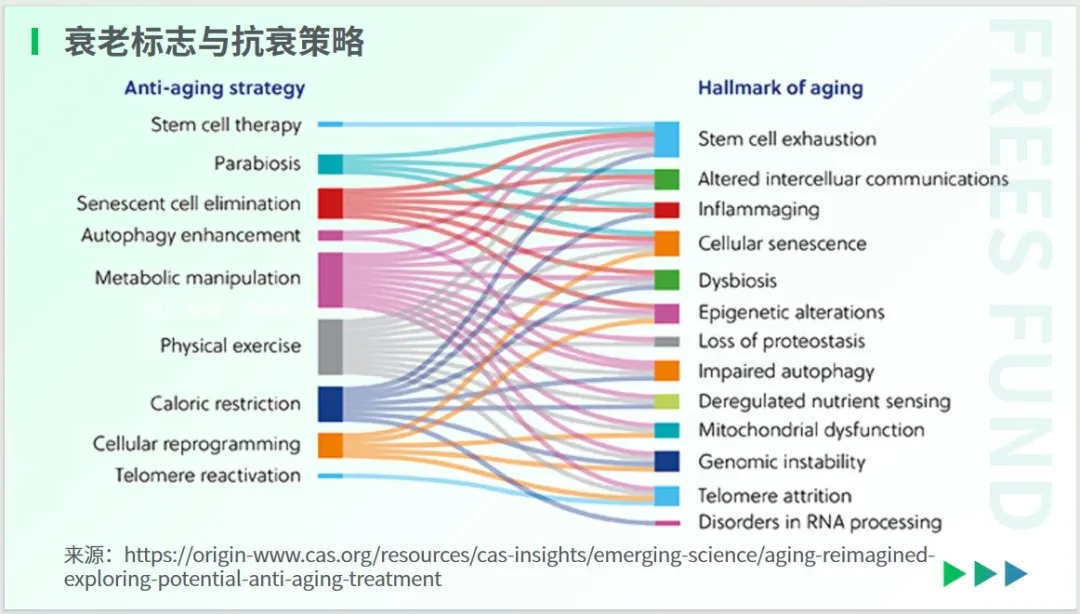
針對上述 12 個衰老標志,研究者們已經展開了許多抗衰策略研究。
從上圖可以看出,體育鍛煉在細胞層面呈現出較好的抗衰老效果,它幾乎與每一個衰老標志都相關聯。類似的,卡路里限制也是一種經過深入研究的抗衰老治療策略,目前有一些臨床試驗正在進行之中。
干細胞治療是針對干細胞耗竭而展開的策略。一些靶向藥的研發是針對線粒體失調、自噬功能失效等標志展開的。其中一個令人興奮的藥物策略是使用衰老細胞毒素,它們能夠選擇性地消除衰老細胞的小分子。
這些旨在解決衰老和衰老相關疾病的策略,可以歸結為三類:行為干預、保健品與醫療。
在行為干預方面,熱量限制、飲食調整、堅持運動、適度寒冷,以及攝入可調節腸道菌群的保健品,這些聽起來或許司空見慣的方法,在理論上都被驗證對抗衰有益。
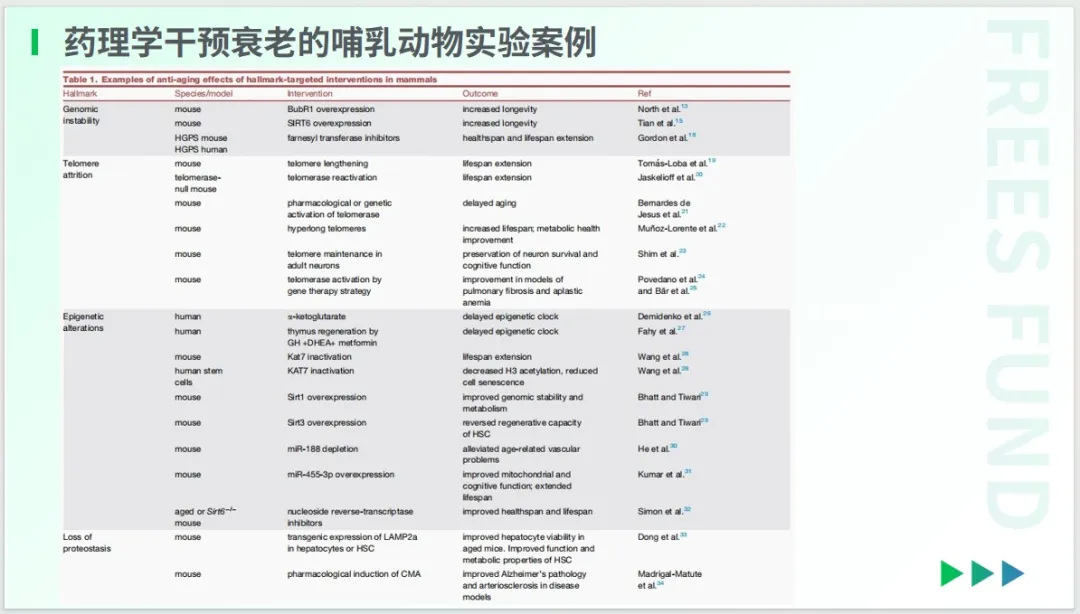
在藥理學干預方面,目前有許多動物實驗的探索,也已經有不少靶點被驗證能夠幫助哺乳動物抗衰。
那么,也許你會好奇,為何還沒有一款真正意義上的抗衰藥呢?這是因為這些在動物實驗中被證明具有潛在有效性的研究成果,尚未能夠進入正規的人體臨床試驗。
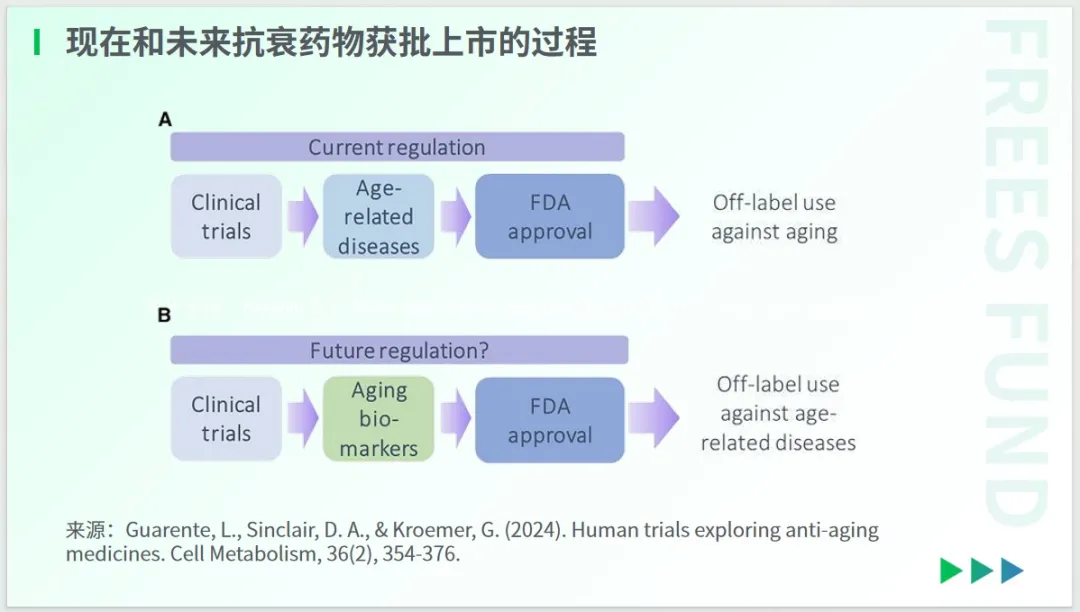
目前,衰老尚未成為公認的藥物開發或治療目標,第一批評估抗衰老干預措施的臨床試驗必須是針對預防或減輕與衰老相關的病癥,而非衰老本身。
這也從側面解釋了為什么著有《長壽》等暢銷書、被譽為哈佛抗衰教父的大衛·辛克萊一度被指賣假藥,從而受到科學界的批評。
未來,隨著“衰老生物標志物”被接受,針對衰老本身的藥物或許能夠得到測試和批準,從而用于治療“衰老”。
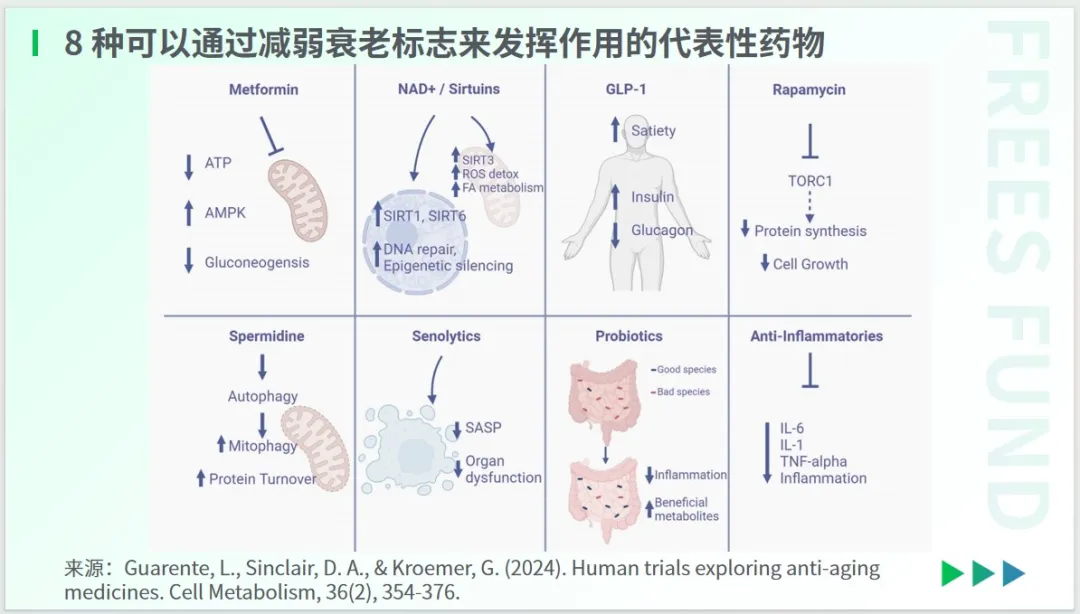
Guarente等學者2024年發表在《Cell Metabolism》上的研究,指出了 8 種可以通過減弱衰老標志來發揮作用的代表性藥物,其中包括用于抗腫瘤和改善神經退行性疾病的免疫抑制劑雷帕霉素(Rapamycin)、被驗證可以用于降糖和減重的藥物GLP-1,以及能促進腸道中有益菌群生長的益生菌,等等。
在這些尚未推向臨床試驗的藥物中,用于治療 2 型糖尿病的藥物二甲雙胍是一個特別的存在。一些動物研究和流行病學數據顯示,二甲雙胍能夠延長壽命,并改善健康狀況。
2015 年,一項名為“使用二甲雙胍靶向衰老”(Targeting Ageing with Metaformin, TAME)的試驗成為 FDA 首個批準將衰老作為治療目標的臨床試驗。
該試驗計劃在 3000 名非糖尿病患者(年齡在 65 - 79 歲之間)中進行雙盲試驗,以研究二甲雙胍的抗衰老作用。目前,TAME 研究仍在進行當中,已有初步證據表明二甲雙胍在延緩衰老方面具備潛力。

人類社會發展到今天,討論抗衰,有許多全新的語境。它不僅關乎每一個個體的命運,還和擺在我們眼前的養老難題有關。而且,如果我們將視野進一步拓寬,它還與人類與 AI 共存、太空探索等中長期命題息息相關。
首先我們來看養老的社會負擔。到 2050 年,全球超過 65 歲的人口將占總人數的六分之一。衰老階段所伴隨的生理功能下降、患病與失能等問題,使得“衰老”已演變為全球性的經濟政策難題。
依據WHO的統計數據,以美國為例,過去 20 年間,美國的人均壽命增長了 2.3%,但其中健康壽命只增長了 0.5%,這表明其“健康壽命”的增長未能與延壽的步伐同步。
與此同時,由于大部分的壽命增長都是處于一種衰老甚至失能狀態,這導致美國人均醫療衛生支出居高不下。
有學者研究指出,使社會和經濟負擔最小化的方式,是讓人口的生存曲線呈現“矩形化”,即讓人口的死亡率更集中在極限壽命附近。當然,這只是理論層面的極端設想。
當我們了解了衰老背后的生物學規律,明白人類預期壽命不會驟然縮短后,問題隨之而來:伴隨老齡化社會而來的種種社會問題,難道真的無藥可解?面對養老金缺口難題,究竟是提高生育率還是抗衰老更為有效?
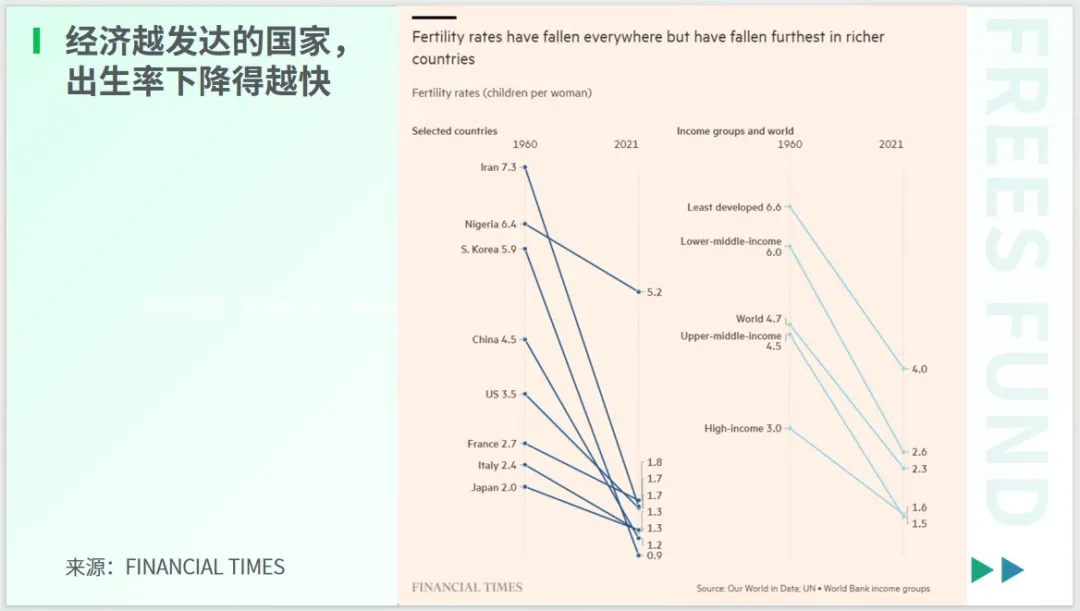
《經濟學人》2024 年 5 月的封面文章指出,當前各個國家和經濟體都對出生率下降的問題深感擔憂。
過去,許多人將其歸因于經濟越發展,人們越不愿意生育。然而,數據顯示,在過去的六十年中,世界上幾乎所有國家的出生率都在下降,且經濟更為發達的國家,出生率下降的速度更快。
這指向了一個我們較少考慮到的維度——隨著人類壽命的延長,人類的出生率必然會下降。
提高生育率與抗衰老,看似是解決方案的“一體兩面”。既然我們難以靠提高出生率來打敗老齡化,或許“抗衰”才是更為直接有效的辦法。換句話說,在人口增長趨緩的時代,通過抗衰延長健康壽命,對推動社會向前發展有積極作用。
再來看人工智能。回望歷史,人類的進步與發展高度依賴群體智慧或者說集體智慧。在古代有文字記錄之前,信息主要靠口耳相傳,老人豐富的閱歷和經驗對群體的生存極具價值。文字被發明后,信息和知識得以被記錄并跨代傳播。
在大模型發展進入快車道的背景下,一個值得深入思考的問題是,人類自身的群體智慧能否跟上 AI 的發展步伐,人類如何在與機器人和 AI 共存的時代實現自身價值,追求更高的目標。
研究表明,人類的大腦在一生中都有可塑性和學習能力。
假如能通過有效的抗衰,延長健康壽命,減少腦疾病,將延長人類大腦發揮作用的時長,有助于人類在衰老過程中保持智力活躍,積累新知與智慧,從而為社會向前發展做出更大的貢獻。
這類似于 AI 大模型的 Scaling Law(規模效應),即更海量、更高質量的數據輸入,會帶來更出色的表現。
此外,懷揣“活得更長、活得更好”的期望,也能讓我們有機會更好地探索太空。人們往返火星一趟需要 969 天的飛行,而旅行者一號飛了 47 年仍未飛出太陽系。
從這個角度看,在奔向星辰大海的旅途中,我們需要通過有效的抗衰來在時間維度上擴展生命。

“衰老”二字,拆分來看,人們更懼怕的是“衰”而非“老”。當我們談及“相守一生”時,會說“與子偕老”,卻對“衰”避而不談。倘若我們終將老去,那么我們所追求的應是“老而不衰”。
因此,研究“抗衰”的目的,簡而言之,即設法在我們的生命中增加健康壽命的比例,減少患病、失能的壽命。
近年來,與抗衰相關的研究開始獲得空前關注,在可預見的未來,這種關注將持續增加。當今科學界對衰老已有較為明確的定義,判斷衰老的指標也從 10 年前的 9 個增至 12 個,未來或許還會有新的補充。
盡管那些動物實驗存在種種局限,但是它們也能間接地為一些非治療型的抗衰方向提供指導,如健康飲食、保持運動以及細胞療法等,這些都值得我們持續關注。
此外,那些原本針對老齡化相關疾病的研究和干預方法,對于抗衰老的指導意義同樣重大。
相信未來幾年,我們將迎來抗衰行業發展的轉折點。屆時,可行的策略和方法可能將變得顯而易見,并推動我們更廣泛地使用干預措施來抵抗衰老。
讓我們一起拭目以待。
參考書單
如果你對衰老和抗衰話題感興趣,可以參考我們整理的“抗衰小書單”。





參考文獻
1. Koonin, E. V. (2012). Does the central dogma still stand?. Biology direct, 7, 1-7.
2. Guo, J., Huang, X., Dou, L., Yan, M., Shen, T., Tang, W., & Li, J. (2022). Aging and aging-related diseases: from molecular mechanisms to interventions and treatments. Signal Transduction and Targeted Therapy, 7(1), 391.
3. Conboy, I. M., Conboy, M. J., Wagers, A. J., Girma, E. R., Weissman, I. L., & Rando, T. A. (2005). Rejuvenation of aged progenitor cells by exposure to a young systemic environment. Nature, 433(7027), 760-764.
4. Reinke, B. A., Cayuela, H., Janzen, F. J., Lema?tre, J. F., Gaillard, J. M., Lawing, A. M., ... & Miller, D. A. (2022). Diverse aging rates in ectothermic tetrapods provide insights for the evolution of aging and longevity. Science, 376(6600), 1459-1466.
5. Scudellari, M. (2015). Blood to blood. Nature, 517(7535), 426.
6. Tartiere, A. G., Freije, J. M., & López-Otín, C. (2024). The hallmarks of aging as a conceptual framework for health and longevity research. Frontiers in Aging, 5, 1334261.
7. Cai, Y., Song, W., Li, J., **g, Y., Liang, C., Zhang, L., ... & Liu, G. H. (2022). The landscape of aging. Science China Life Sciences, 65(12), 2354-2454.
8. López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M., & Kroemer, G. (2023). Hallmarks of aging: An expanding universe. Cell, 186(2), 243-278.
9. Guarente, L., Sinclair, D. A., & Kroemer, G. (2024). Human trials exploring anti-aging medicines. Cell Metabolism, 36(2), 354-376.
10. López-Otín, C., Pietrocola, F., Roiz-Valle, D., Galluzzi, L., & Kroemer, G. (2023). Meta-hallmarks of aging and cancer. Cell metabolism, 35(1), 12-35.
向上滑動閱覽